Фото: Shutterstock/FOTODOM
30 июня 2017 года, 09:18
Комментировать
Читать еще:
гастрит, рак желудка, язва желудка
Заражение этой инфекцией — основная причина гастрита, язвенной болезни желудка и двенадцатиперстной кишки. ВОЗ признала связь между Helicobacter pylori (Хеликобактер) и раком желудка и занесла эту бактерию в разряд достоверных канцерогенов. Кроме того, Helicobacter pylori может запускать аутоиммунные процессы, установлена ее взаимосвязь и с некоторыми кожными заболеваниями. О том, что надо знать о коварной бактерии, рассказывает эксперт Центра молекулярной диагностики (CMD) ЦНИИ Эпидемиологии Роспотребнадзора Марина Вершинина.
 Марина Вершинина. Фото: из личного архива
Марина Вершинина. Фото: из личного архива
Что такое Хеликобактер
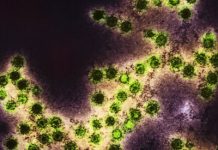
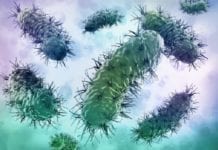
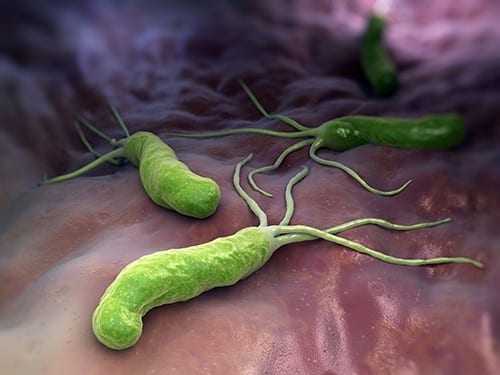
Микроскопический, но коварный враг нашего желудка Хеликобактер — это спиралевидная грамотрицательная бактерия, за открытие которой австралийским медикам Барри Маршаллу и Роберту Уоррену в 2005 году присудили Нобелевскую премию в области медицины. По некоторым данным, более половины населения планеты инфицировано этой бактерией. Хеликобактер обладает уникальной способностью колонизировать слизистую оболочку желудка и выживать в условиях высокой кислотности, что чревато развитием у человека гастрита и язвенной болезни. Кроме того, в соответствии с классификацией Международного Агентства по Изучению рака (IARC), Хеликобактер является достоверным канцерогеном и может приводить к развитию рака желудка. Считается, что она проникает в организм с зараженной водой или едой, передается при тесном физическом контакте с зараженным человеком, через слюну, а также при использовании общей посуды и предметов гигиены.
Почему эта бактерия такая живучая
В норме желудочный сок имеет резко кислую реакцию, необходимую для переваривания пищи (натощак на поверхности эпителия рН составляет 1,5-2,0). Но Хеликобактер приспособилась к выживанию в агрессивной среде желудка и при помощи своих жгутиков свободно передвигается в слизи, выстилающей его стенки. Еще один фактор, повышающий устойчивость коварной бактерии — ее способность образовывать микробные биопленки, охраняющие от воздействия антибиотиков и механизмов иммунной защиты носителя.
Вредоносная жизнедеятельность
После инфицирования Хеликобактер быстро преодолевает защитный слой и колонизирует слизистую оболочку желудка. Обосновавшись там, бактерия начинает выработку уреазы — особого фермента, расщепляющего мочевину пищевых продуктов с образованием аммиака. Аммиак нейтрализует соляную кислоту желудка и обеспечивает бактерии локальное поддержание комфортного для нее pH (около 6–7). Это приводит к раздражению слизистой желудка, вызывает ее воспаление, а затем и гибель клеток желудочного эпителия.
С другой стороны, чтобы преодолеть защелачивание среды и восстановить нормальную кислотность, в желудке происходит увеличение секреции гормона гастрина, повышается продукция соляной кислоты и пепсина, снижется уровень бикарбонатов. Эпителиальная оболочка, лишенная защитного слоя слизи под действием ферментов бактерий, становится уязвимой для собственной соляной кислоты и пепсина. Это также приводит к воспалению и изъязвлению тканей.
Основные симптомы
В числе основных симптомов поражения желудочно-кишечного тракта: нарушение аппетита и потеря веса, боли в разных отделах живота и за грудиной после употребления пищи, тошнота и ощущения давления в подложечной области, метеоризм и урчание в животе, чувство тяжести после еды и отрыжка с кислым привкусом и запахом тухлых яиц, изменения в работе кишечника — запоры или поносы.
Не только желудок
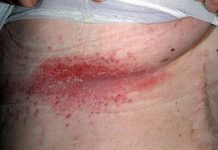
Ученые обнаружили взаимосвязь хеликобактерной инфекции с некоторыми болезнями кожи, среди которых хроническая крапивница, атопический дерматит, розацеа (розовые угри). Предполагается также, что Хеликобактер оказывает существенное влияние на патологический процесс при угревой сыпи (акне), псориазе, красном плоском лишае и многих других дерматологических и системных заболеваниях.
Этому есть несколько возможных объяснений. Во-первых, из-за деятельности бактерии повышается проницаемость слизистой оболочки желудочно-кишечного тракта, и человек становится более восприимчив к пищевым аллергенам. Кроме того, не исключено, что Хеликобактер пилори и сама является аллергеном.
Во-вторых, в процессе жизнедеятельности бактерии вырабатывается большое количество агрессивных веществ. Увеличивается концентрация оксида азота (NO) в сыворотке крови и тканях. Это может стать причиной расширения сосудов, повышения проницаемости сосудистой стенки, покраснения кожи.
В-третьих, Хеликобактер способна запускать каскад иммунных реакций, в результате которых может происходить выработка антител против собственных клеток и тканей человека.
И, наконец, не стоит забывать и об участии возбудителя в нарушении обменных процессов. Инфицирование Хеликобактер может привести к развитию железодефицитных состояний и авитаминозов, что также ведет к ухудшению состояния кожи, волос и ногтей.
Диагностика
Хеликобактер является далеко не единственной причиной заболеваний желудка. Патологические изменения в слизистой оболочке желудка могут возникать под влиянием многих факторов: генетической предрасположенности, стресса, нерационального питания, вредных привычек. Гастрит и язву желудка может вызвать прием некоторых лекарственных препаратов. Поэтому для назначения адекватной терапии необходима точная диагностика.
На сегодняшний день существует несколько видов анализов, позволяющих диагностировать хеликобактерную инфекцию: определение антител к Helicobacter pylori в венозной крови, уреазный дыхательный тест (УДТ) и анализ на антигены Helicobacter pylori в кале.
Определение антител (иммуноглобулинов Ig G и Ig A) в крови может применяться как скрининговое (первичное) лабораторное исследование. Положительный результат («антитела обнаружены») может свидетельствовать как о текущей инфекции, так и об инфекции, перенесенной в прошлом. Выработка антител — это защитная реакция системы иммунитета на присутствие возбудителя, поэтому повышенный уровень иммуноглобулинов может довольно длительно сохраняться в крови и после выздоровления. Поэтому в случае обнаружения антител к Helicobacter pylori, для уточнения диагноза необходимо провести уреазный дыхательный тест (УДТ) или определение антигена в кале.
В мировой практике основным референсным методом диагностики является уреазный дыхательный тест. Этот тест рекомендован при неблагоприятной семейной истории заболеваний желудочно-кишечного тракта, частом применении нестероидных противовоспалительных препаратов или при наличии необъяснимой железодефицитной анемии. В нашей стране до недавнего времени этот анализ был малодоступен и проводился только в стационарных условиях. Однако методика проведения теста довольно проста.
Для исследования у пациента берут две пробы выдыхаемого воздуха: натощак и через несколько минут после приема специального раствора. Анализ выдыхаемого воздуха позволяет выявить присутствие выделяемой Хеикобактером уреазы, что свидетельствует о наличии активной бактериальной инфекции в желудке. Отрицательный результат уреазного дыхательного теста через четыре недели после проведенного лечения свидетельствует об эрадикации (уничтожении) бактерии.
Определение антигенов Helicobacter pylori в кале — также простое, быстрое и безопасное исследование. Анализ основан на способности искусственно синтезированных антител прочно связываться с определенными участками (антигенами) на поверхности бактерии. Если Хеликобактер присутствует в кале пациента, происходит реакция между антигенами Helicobacter pylori и антителами в составе реагента, нанесенного на нитроцеллюлозную мембрану. Это приводит к появлению второй окрашенной полосы в строго определенной зоне (по аналогии с тестами на бумажных полосках). Результат оценивают визуально: наличие двух окрашенных полос свидетельствует о положительном результате («антиген обнаружен»), единственная полоса говорит об отсутствии антигенов в кале, и, следовательно, позволяет исключить активное течение инфекции. Это достаточно точный метод, который характеризуется высокой чувствительностью и специфичностью (90% и более). Анализ по определению антигенов Helicobacter pylori в кале особенно удобен в детской практике, так как собрать выдыхаемый воздух у маленького ребенка технически трудновыполнимо.
Лечение
Установление бактериальной природы гастрита и язвы желудка, и включение в схему лечения антибиотиков позволило добиться в последние двадцать лет впечатляющих успехов. В целом, на сегодняшний день разработано несколько эффективных схем эрадикационной терапии, сочетающих применение антибактериальных средств и препаратов, воздействующих на секрецию соляной кислоты. В соответствии с V Маастрихтским соглашением, длительность курса терапии должна составлять 14 дней.
Обязательное условие успешности лечения гастрита и язвенной болезни — соблюдение щадящей диеты, исключающей употребление продуктов, повышающих выработку соляной кислоты (овощных, мясных и рыбных блюд в жареном виде, консервов, пряностей, алкоголя и газированных напитков, кофе, крепкого чая, черного хлеба) или вызывающих механическое раздражение желудка (овощей, богатых клетчаткой, фруктов с кожурой, хлеба грубого помола). По мере стихания обострения диета постепенно расширяется. Но соблюдать рекомендации по здоровому питанию следует на протяжении всей жизни — это основной способ профилактики возможных обострений.