Содержание
- Система свертывания крови (гемостаза)
- Эндотелиальные клетки
- Поддержание жидкого состояния крови
- Простациклин
- Окись азота (NO) и АДФаза
- Система протеина С
- Патология системы протеина С
- Фульминантная пурпура
- Тромбозы
- V фактор Leiden
- Патология системы протеина С
- Ингибитор тканевого тромбопластина
- Глюкозаминогликаны (гепарин, антитромбин III, кофактор гепарина II)
- Процесс свертывания крови — тромбообразования
- Системы и факторы свертывания крови
- Тромбопластин
- Цитокины
- Тромбоциты
- Тромбоцитарный гемостаз
- Плазменные факторы свертывания крови
- Система адгезивных молекул плазмы
- Фактор Виллебранда
- Фибриноген — фактор I
- Плазменный фибронектин
- Тромбоспондин
- Витронектин
- Факторы свертывания крови
- Система фибринолиза
- Внутренний механизм активации
- Внешний механизм активации
- Система первичных и вторичных антикоагулянтов-антипротеаз
- Система первичных репарантов-заживителей
- Система адгезивных молекул плазмы
- Механизм свертывания крови
- Внутренний путь свертывания крови
- Внешний путь свертывания крови
- Механизм свертывания крови кратко
Процесс свертывания крови начинается с кровопотери, но массивная кровопотеря, сопровождающаяся падением артериального давления, ведет к резким изменениям всей системы гемостаза.
Система свертывания крови (гемостаза)
Система свертывания крови — это сложный многокомпонентный комплекс гомеостаза человека, обеспечивающий сохранение целостности организма благодаря постоянному поддержанию жидкого состояния крови и формированию при необходимости различного типа тромбов, а также активации процессов заживления в местах сосудистых и тканевых повреждений.
Функционирование системы свертывания обеспечивается непрерывным взаимодействием сосудистой стенки и циркулирующей крови. Известны определенные компоненты, отвечающие за нормальную деятельность коагулологической системы:
- эндотелиальные клетки сосудистой стенки,
- тромбоциты,
- адгезивные молекулы плазмы,
- плазменные факторы свертывания,
- системы фибринолиза,
- системы физиологических первичных и вторичных антикоагулянтов-антипротеаз,
- плазменная система физиологических первичных репарантов-заживителей.
Любые повреждения сосудистой стенки, «травмирование крови», с одной стороны, приводят к различной тяжести кровотечениям, а с другой — вызывают физиологические, а в последующем патологические изменения в системе гемостаза, которые способны сами по себе привести к гибели организма. К закономерным тяжелым и частым осложнениям массивной кровопотери относится острый синдром диссеминированного внутрисосудистого свертывания (острый ДВС-синдром).
При острой массивной кровопотере, а ее нельзя представить без повреждения сосудов, практически всегда имеет место локальный (в месте повреждения) тромбоз, который в сочетании с падением артериального давления может запустить острый ДВС-синдром, являющийся важнейшим и патогенетически наиболее неблагоприятным механизмом всех бед острой массивной кровопотери.
Эндотелиальные клетки
Эндотелиальные клетки сосудистой стенки обеспечивают поддержание жидкого состояния крови, непосредственно влияя на многие механизмы и звенья тромбообразования, полностью блокируя или эффективно сдерживая их. Сосуды обеспечивают ламинарность тока крови, что препятствует склеиванию клеточных и белковых компонентов.
Эндотелий несет на своей поверхности отрицательный заряд, как и циркулирующие в крови клетки, различные гликопротеины и другие соединения. Одноименно заряженные эндотелий и циркулирующие элементы крови отталкиваются, что препятствует слипанию клеток и белковых структур в циркуляторном русле.
Поддержание жидкого состояния крови
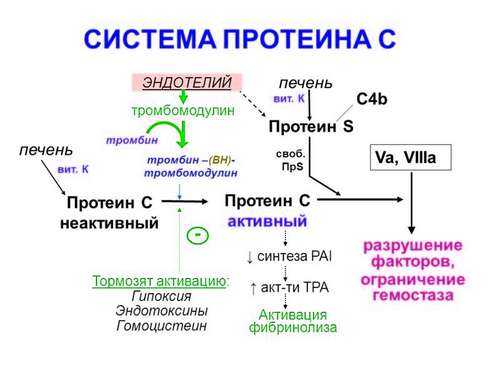 Схема системы протеина С
Схема системы протеина С
Поддержанию жидкого состояния крови способствуют:
- простациклин (PGI2),
- NO и АДФаза,
- система протеина С,
- ингибитор тканевого тромбопластина,
- глюкозаминогликаны и, в частности, гепарин, антитромбин III, кофактор гепарина II, тканевой активатор плазминогена и др.
Простациклин
Блокада агглютинации и агрегации тромбоцитов в кровотоке осуществляется несколькими путями. Эндотелий активно вырабатывает простагландин I2 (PGI2), или простациклин, который ингибирует формирование первичных агрегатов тромбоцитов. Простациклин способен «разбивать» ранние агглютинаты и агрегаты тромбоцитов, вместе с тем являясь вазодилататором.
Окись азота (NO) и АДФаза
Дезагрегация тромбоцитов и вазодилатация осуществляются также путем выработки эндотелием окиси азота (NO) и так называемой АДФазы (фермента, расщепляющего аденозиндифосфат — АДФ) — соединения, вырабатываемого различными клетками и являющегося активным агентом, стимулирующим агрегацию тромбоцитов.
Система протеина С
Сдерживающее и ингибирующее влияние на свертывающую систему крови, преимущественно на ее внутренний путь активации, оказывает система протеина С. В комплекс этой системы входят:
Эндотелиальные клетки вырабатывают тромбомодулин, который при участии тромбина активирует протеин С, переводя его соответственно в протеин Ca. Активированный протеин Са при участии протеина S инактивирует факторы Va и VIIIa, подавляя и ингибируя внутренний механизм свертывающей системы крови. Кроме того, активированный протеин Са стимулирует активность системы фибринолиза двумя путями: за счет стимуляции выработки и выброса из эндотелиальных клеток в кровоток тканевого активатора плазминогена, а также благодаря блокаде ингибитора тканевого активатора плазминогена (PAI-1).
Патология системы протеина С
Нередко наблюдаемая наследственная или приобретенная патология системы протеина С приводит к развитию тромботических состояний.
Фульминантная пурпура
Гомозиготный дефицит протеина С (фульминантная пурпура) — крайне тяжелая патология. Дети с фульминантной пурпурой практически нежизнеспособны и погибают в раннем возрасте от тяжелых тромбозов, острого ДВС-синдрома и сепсиса.
Тромбозы
Гетерозиготный наследственный дефицит протеина С или протеина S способствует возникновению тромбозов у молодых. Чаще наблюдаются тромбозы магистральных и периферических вен, тромбоэмболии легочной артерии, ранние инфаркты миокарда, ишемические инсульты. У женщин с дефицитом протеина С или S, принимающих гормональные контрацептивы, риск тромбозов (чаше тромбозов мозговых сосудов) возрастает в 10—25 раз.
Поскольку протеины С и S являются витамин К-зависимыми протеазами, вырабатываемыми в печени, лечение тромбозов непрямыми антикоагулянтами типа синкумара или пелентана у пациентов с наследственным дефицитом протеина С или S может приводить к усугублению тромботического процесса. Кроме того, у ряда больных при проведении лечения непрямыми антикоагулянтами (варфарином) могут развиваться периферические некрозы кожи («варфариновые некрозы»). Их появление практически всегда означает наличие гетерозиготною дефицита протеина С, что ведет к снижению фибринолитической активности крови, локальной ишемии и кожным некрозам.
V фактор Leiden
Еще одна патология, напрямую связанная с функционированием системы протеина С, получила название наследственной резистентности к активированному протеину С, или V фактор Leiden. По сути V фактор Leiden представляет собой мутантный V фактор с точечной заменой аргинина в 506-й позиции фактора V на глутамин. V фактор Leiden обладает повышенной резистентностью к прямому действию активированного протеина С. Если наследственный дефицит протеина С у пациентов преимущественно с венозными тромбозами встречается в 4-7% случаев, то V фактор Leiden, по данным разных авторов, — в 10—25%.
Ингибитор тканевого тромбопластина
Эндотелий сосудов также может ингибировать тромбообразование при активации свертывания крови по внешнему механизму. Эндотелиальные клетки активно вырабатывают ингибитор тканевого тромбопластина, который инактивирует комплекс тканевый фактор — фактор VIIa (ТФ—VIIa), что приводит к блокаде внешнего механизма свертывания крови, активизирующегося при попадании тканевого тромбопластина в кровоток, тем самым поддерживая текучесть крови в циркуляторном русле.
Глюкозаминогликаны (гепарин, антитромбин III, кофактор гепарина II)
Другой механизм поддержания жидкого состояния крови связан с выработкой эндотелием различных глюкозаминогликанов, среди которых известны гепаран- и дерматан-сульфат. Эти глюкозаминогликаны по строению и функциям близки к гепаринам. Вырабатываемый и выбрасываемый в кровоток гепарин связывается с циркулирующими в крови молекулами антитромбина III (AT III), активируя их. В свою очередь активированный AT III захватывает и инактивирует фактор Ха, тромбин и ряд других факторов свертывающей системы крови. Кроме механизма инактивации свертывания, осуществляющегося через АТ III, гепарины активируют так называемый кофактор гепарина II (КГ II). Активированный КГ II, как и AT III, ингибирует функции фактора Ха и тромбина.
Кроме влияния на активность физиологических антикоагулянтов-антипротеаз (AT III и КГ II), гепарины способны модифицировать функции таких адгезивных молекул плазмы, как фактор Виллебранда и фибронектин. Гепарин снижает функциональные свойства фактора Виллебранда, способствуя уменьшению тромботического потенциала крови. Фибронектин в результате гепариновой активации связывается с различными объектами—мишенями фагоцитоза — клеточными мембранами, тканевым детритом, иммунными комплексами, фрагментами коллагеновых структур, стафилококками и стрептококками. Вследствие стимулированных гепарином опсонических взаимодействий фибронектина активизируется инактивация мишеней фагоцитоза в органах макрофагальной системы. Очистка циркуляторного русла от объектов-мишеней фагоцитоза способствует сохранению жидкого состояния и текучести крови.
Кроме того, гепарины способны стимулировать выработку и выброс в циркуляторное русло ингибитора тканевого тромбопластина, что существенно снижает вероятность тромбоза при внешней активации свертывающей системы крови.
Процесс свертывания крови — тромбообразования
Вместе с описанным выше существуют механизмы, также связанные с состоянием сосудистой стенки, но не способствующие поддержанию жидкого состояния крови, а ответственные за ее свертывание.
Процесс свертывания крови начинается с повреждения целостности сосудистой стенки. При этом различают внутренний и внешний механизмы процесса формирования тромба.
При внутреннем механизме повреждение только эндотелиального слоя сосудистой стенки приводит к тому, что поток крови контактирует со структурами субэндотелия — с базальной мембраной, в которой основными тромбогенными факторами являются коллаген и ламинин. С ними взаимодействуют находящиеся в крови фактор Виллебранда и фибронектин; формируется тромбоцитарный тромб, а затем — фибриновый сгусток.
Необходимо отметить, что тромбы, формирующиеся в условиях быстрого кровотока (в артериальной системе), могут существовать практически только при участии фактора Виллебранда. Напротив, в формировании тромбов при относительно небольших скоростях кровотока (в микроциркуляторном русле, венозной системе) участвуют как фактор Виллебранда, так и фибриноген, фибронектин, тромбоспондин.
Другой механизм тромбообразования осуществляется при непосредственном участии фактора Виллебранда, который при повреждении целостности сосудов существенно увеличивается в количественном отношении вследствие поступления из телец Вейбола-Паллада эндотелия.
Системы и факторы свертывания крови
Тромбопластин
Важнейшую роль во внешнем механизме тромбообразования играет тканевый тромбопластин, поступающий в кровоток из интерстициального пространства после разрыва целостности сосудистой стенки. Он индуцирует тромбообразование, активируя свертывающую систему крови при участии VII фактора. Поскольку тканевый тромбопластин содержит фосфолипидную часть, тромбоциты в этом механизме тромбообразования участвуют мало. Именно появление тканевого тромбопластина в русле крови и его участие в патологическом тромбообразовании и определяют развитие острого ДВС-синдрома.
Цитокины
Следующий механизм тромбообразования реализуется с участием цитокинов — интерлейкина-1 и интерлейкина-6. Образующийся в результате их взаимодействия фактор некроза опухоли стимулирует выработку и выброс из эндотелия и моноцитов тканевого тромбопластина, о значении которого уже говорилось. Этим объясняется развитие локальных тромбов при различных заболеваниях, протекающих с четко выраженными воспалительными реакциями.
Тромбоциты
Специализированными клетками крови, участвующими в процессе ее свертывания, являются тромбоциты — безъядерные клетки крови, представляющие собой фрагменты цитоплазмы мегакариоцитов. Продукция тромбоцитов связана с определенным цитокином — тромбопоэтином, регулирующим тромбоцитопоэз.
Количество тромбоцитов в крови составляет 160-385×109/л. Они хорошо видны в световом микроскопе, поэтому при проведении дифференциальной диагностики тромбозов или кровоточивости микроскопия мазков периферической крови необходима. В норме размер тромбоцита не превышает 2-3,5 мкм (около ⅓-¼ диаметра эритроцита). При световой микроскопии неизмененные тромбоциты выглядят как округлые клетки с ровными краями и красно-фиолетовыми гранулами (α-гранулы). Продолжительность жизни тромбоцитов составляет в среднем 8-9 сут. В норме они дискоидной формы, но при активации принимают форму сферы с большим количеством цитоплазматических выпячиваний.
В тромбоцитах имеется 3 типа специфических гранул:
- лизосомы, содержащие в большом количестве кислые гидролазы и другие ферменты;
- α-гранулы, содержащие множество различных белков (фибриноген, фактор Виллебранда, фибронектин, тромбоспондин и др.) и окрашивающиеся по Романовскому-Гимзе в фиолетово-красный цвет;
- δ-гранулы — плотные гранулы, содержащие большое количество серотонина, ионов К+, Ca2+, Mg2+ и др.
В α-гранулах содержатся строго специфичные белки тромбоцитов — такие, как 4-й пластиночный фактор и β-тромбоглобулин, являющиеся маркерами активации тромбоцитов; их определение в плазме крови может помочь в диагностике текущих тромбозов.
Кроме того, в структуре тромбоцитов имеются система плотных трубочек, являющаяся как бы депо для ионов Ca2+, а также большое количество митохондрий. При активации тромбоцитов происходит ряд биохимических реакций, которые при участии циклооксигеназы и тромбоксансинтетазы приводят к образованию тромбоксана А2 (ТХА2) из арахидоновой кислоты — мощного фактора, отвечающего за необратимую агрегацию тромбоцитов.
Тромбоцит покрыт 3-слойной мембраной, на внешней ее поверхности располагаются различные рецепторы, многие из которых являются гликопротеинами и взаимодействуют с различными белками и соединениями.
Тромбоцитарный гемостаз
Рецептор гликопротеина Iа связывается с коллагеном, рецептор гликопротеина Ib взаимодействует с фактором Виллебранда, гликопротеинами IIb-IIIa — с молекулами фибриногена, хотя может связываться и с фактором Виллебранда, и с фибронектином.
При активации тромбоцитов агонистами — АДФ, коллагеном, тромбином, адреналином и др. — на их внешней мембране появляется 3-й пластиночный фактор (мембранный фосфолипид), активирующий скорость свертывания крови, повышая ее в 500-700 тыс. раз.
Плазменные факторы свертывания крови
Плазма крови содержит несколько специфических систем, участвующих в каскаде свертывания крови. Это системы:
- адгезивных молекул,
- факторов свертывания крови,
- факторов фибринолиза,
- факторов физиологических первичных и вторичных антикоагулянтов-антипротеаз,
- факторов физиологических первичных репарантов-заживителей.
Система адгезивных молекул плазмы
Система адгезивных молекул плазмы представляет собой комплекс гликопротеинов, отвечающих за межклеточные, клеточно-субстратные и клеточно-белковые взаимодействия. К ней относятся:
Фактор Виллебранда
Фактор Виллебранда высокомолекулярный гликопротеин с молекулярной массой 103 кД и более. Фактор Виллебранда выполняет множество функций, но основные из них две:
- взаимодействие с VIII фактором, благодаря чему происходит защита антигемофильного глобулина от протеолиза, что увеличивает продолжительность его жизни;
- обеспечение процессов адгезии и агрегации тромбоцитов в циркуляторном русле, особенно при высоких скоростях кровотока в сосудах артериальной системы.
Снижение уровня фактора Виллебранда ниже 50%, наблюдающееся при болезни или синдроме Виллебранда, приводит к выраженной петехиальной кровоточивости, как правило, микроциркуляторного типа, проявляющейся синяковостью при небольших травмах. Однако при тяжелой форме болезни Виллебранда может наблюдаться гематомный тип кровоточивости, подобный гемофилии (кровоизлияние в полость сустава).
Напротив, существенное повышение концентрации фактора Виллебранда (более 150%) может приводить к тромбофилическому состоянию, что нередко клинически проявляется различного типа тромбозами периферических вен, инфарктом миокарда, тромбозами системы легочной артерии или мозговых сосудов.
Фибриноген — фактор I
Фибриноген, или фактор I, участвует во многих межклеточных взаимодействиях. Его основными функциями являются участие в формировании фибринового тромба (армирование тромба) и осуществление процесса агрегации тромбоцитов (прикрепление одних тромбоцитов к другим) благодаря специфическим тромбоцитарным рецепторам гликопротеинов IIb-IIIа.
Плазменный фибронектин
Плазменный фибронектин — адгезивный гликопротеин, взаимодействующий с различными факторами свертывания крови.Также одной из функций плазменного фибронектина является репарация дефектов сосудов и тканей. Показано, что нанесение фибронектина на участки тканевых дефектов (трофические язвы роговицы глаза, эрозии и язвы кожных покровов) способствует стимуляции репаративных процессов и более быстрому заживлению.
Нормальная концентрация плазменного фибронектина в крови — около 300 мкг/мл. При тяжелых травмах, массивной кровопотере, ожогах, длительных полостных операциях, сепсисе, остром ДВС-синдроме в результате потребления уровень фибронектина падает, что снижает фагоцитарную активность макрофагальной системы. Именно этим можно объяснить высокую частоту инфекционных осложнений у лиц, перенесших массивную кровопотерю, и целесообразность назначения пациентам переливания криопреципитата или свежезамороженной плазмы, содержащих в большом количестве фибронектин.
Тромбоспондин
Основными функциями тромбоспондина являются обеспечение полноценной агрегации тромбоцитов и связывание их с моноцитами.
Витронектин
Витронектин, или белок, связывающийся со стеклом, участвует в нескольких процессах. В частности, он связывает комплекс АТ III-тромбин и в дальнейшем выводит его из циркуляции через макрофагальную систему. Кроме того, витронектин блокирует клеточно-литическую активность конечного каскада факторов системы комплемента (комплекс С5-С9), тем самым препятствуя реализации цитолитического эффекта активации системы комплемента.
Факторы свертывания крови
Система плазменных факторов свертывания крови — это сложный многофакторный комплекс, активация которого приводит к формированию стойкого фибринового сгустка. Она играет основную роль в остановке кровотечения при всех вариантах повреждения целостности сосудистой стенки.
Система фибринолиза
Система фибринолиза является важнейшей системой, препятствующей бесконтрольному свертыванию крови. Активация системы фибринолиза реализуется по внутреннему либо по внешнему механизму.
Внутренний механизм активации
Внутренний механизм активации фибринолиза начинается с активации плазменного XII фактора (фактора Хагемана) при участии высокомолекулярного кининогена и калликреин-кининовой системы. В результате плазминоген переходит в плазмин, который расщепляет молекулы фибрина на мелкие фрагменты (X, Y, D, Е), опсоннзируюшиеся плазменным фибронектмном.
Внешний механизм активации
Внешний путь активации фибринолитической системы может осуществляться стрептокиназой, урокиназой либо тканевого активатора плазминогена. Внешний путь активации фибринолиза часто используется в клинической практике для лизирования острых тромбозов различной локализации (при тромбоэмболии легочной артерии, остром инфаркте миокарда и др.).
Система первичных и вторичных антикоагулянтов-антипротеаз
Система физиологических первичных и вторичных антикоагулянтов-антипротеаз существует в организме человека для инактивации различных протеаз, плазменных факторов свертывания и многих компонентов фибринолитической системы.
К первичным антикоагулянтам относится система, включающая гепарин, AT III и КГ II. Эта система преимущественно ингибирует тромбин, фактор Ха и ряд других факторов свертывающей системы крови.
Система протеина С, как уже отмечалось, ингибирует Va и VIIIa плазменные факторы свертывания, что в итоге тормозит свертывание крови по внутреннему механизму.
Система ингибитора тканевого тромбопластина и гепарин ингибируют внешний путь активации свертывания крови, а именно комплекс ТФ-VII фактор. Гепарин в этой системе играет роль активатора выработки и выброса в кровоток ингибитора тканевого тромбопластинаиз эндотелия сосудистой стенки.
PAI-1 (ингибитор тканевого активатора плазминогена) является основной антипротеазой, инактивирующей активность тканевого активатора плазминогена.
К физиологическим вторичным антикоагулянтам-антипротеазам относятся компоненты, концентрация которых повышается в процессе свертывания крови. Одним из основных вторичных антикоагулянтов является фибрин (антитромбин I). Он активно сорбирует на своей поверхности и инактивирует циркулирующие в кровотоке свободные молекулы тромбина. Инактивировать тромбин могут также дериваты факторов Va и VIIIa. Кроме того, в крови тромбин инактивируют циркулирующие молекулы растворимого гликокалицина, которые представляют собой остатки рецептора тромбоцитов гликопротеина Ib. В составе гликокалицина имеется определенная последовательность — «ловушка» для тромбина. Участие растворимого гликокалицина в инактивации циркулирующих молекул тромбина позволяет достигать самоограничения тромбообразования.
Система первичных репарантов-заживителей
В плазме крови находятся определенные факторы, которые способствуют процессам заживления и репарации сосудистых и тканевых дефектов, — так называемая физиологическая система первичных репарантов-заживителей. В эту систему входят:
- плазменный фибронектин,
- фибриноген и его производное фибрин,
- трансглутаминаза или XIII фактор свертывающей системы крови,
- тромбин,
- фактор роста тромбоцитов — тромбопоэтин.
О роли и значении каждого из этих факторов в отдельности уже говорилось.
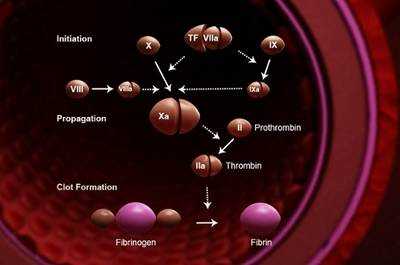
Механизм свертывания крови
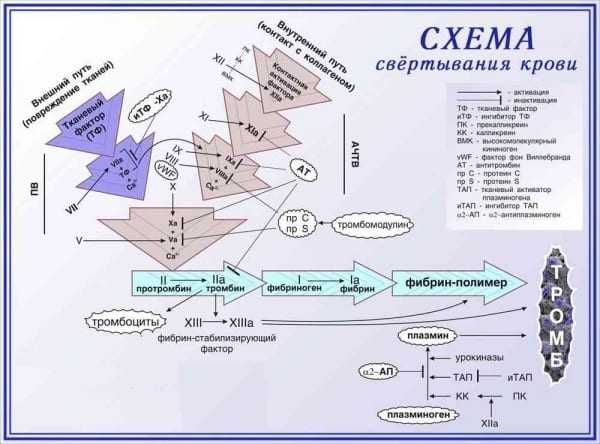 Схема свертывания крови
Схема свертывания крови
Выделяют внутренний и внешний механизм свертывания крови.
Внутренний путь свертывания крови
Во внутреннем механизме свертывания крови участвуют факторы, находящиеся в крови в нормальных условиях.
По внутреннему пути процесс свертывания крови начинается с контактной или протеазной активации XII фактора (или фактора Хагемана) при участии высокомолекулярного кининогена и калликреин-кининовой системы.
⇓
XII фактор превращается в XIIа (активированный) фактор, который активирует XI фактор (предшественник плазменного тромбопластина), переводя его в фактор ХIа.
⇓
Последний активирует IX фактор (антигемофилический фактор В, или фактор Кристмаса), переводя его при участии фактора VIIIa (антигемофилический фактор А) в фактор IХа. В активации IX фактора участвуют ионы Ca2+ и 3-й тромбоцитарный фактор.
⇓
Комплекс факторов IХа и VIIIa с ионами Ca2+ и 3-м тромбоцитарным фактором активирует X фактор (фактор Стюарта), переводя его в фактор Ха. В активации X фактора принимает также участие фактор Va (проакцелерин).
⇓
Комплекс факторов Ха, Va, ионов Са (IV фактор) и 3-го тромбоцитарного фактора называется протромбиназой; она активирует протромбин (или II фактор), превращая его в тромбин.
⇓
Последний расщепляет молекулы фибриногена, переводя его в фибрин.
⇓
Фибрин из растворимой формы под влиянием фактора XIIIа (фибринстабилизирующий фактор) превращается в нерастворимый фибрин, который непосредственно и осуществляет армирование (укрепление) тромбоцитарного тромба.
Внешний путь свертывания крови
Внешний механизм свертывания крови осуществляется при попадании в циркуляторное русло из тканей тканевого тромбопластина (или III, тканевого, фактора).
Тканевый тромбопластин связывается с VII фактором (проконвертином), переводя его в фактор VIIa.
⇓
Последний активирует X фактор, переводя его в фактор Ха.
Дальнейшие превращения свертывающего каскада такие же, как при активации плазменных факторов свертывания по внутреннему механизму.
Механизм свертывания крови кратко
В целом механизм свертывания крови кратко может быть представлен как ряд последовательных этапов:
При острой массивной кровопотере, осложненной шоком, равновесие в системе гемостаза, а именно между механизмами тромбообразования и фибринолиза быстро нарушается, так как потребление существенно превосходит продукцию. Развивающееся истощение механизмов свертывания крови и является одним из звеньев развития острого ДВС-синдрома.