Раз в университете я летом устроился поработать по ночам в аптеке. Как-то вечером заходит женщина за пачкой антибиотика. Выдаю ей препарат и прощаюсь. Мимо проходит задержавшаяся на работе заведующая аптекой. Останавливается и со словами «Молодой человек, отойдите-ка» обращается к покупательнице: «Милочка, а что, для защиты от диареи ничего брать не будем? Значит так: вот пачка пробиотика (полезных бактерий), вот флуконазол от грибка и антигистаминное. Иммунитет тоже надо поддержать, такая нагрузка, возьмите иммуностимулятор». И так я с открытым ртом проводил покупательницу с пачкой антибиотика за триста рублей и мешком препаратов еще тысячи на две, выданных ей «в догонку». Типичная ситуация, правда?
Конечно. А разве можно обойтись без «профилактики»?
В большинстве случаев можно. По крайней мере, действующие клинические руководства — коллегии гастроэнтерологов США (ACG) и общества инфекционистов США (IDSA), а также других организаций — не предписывают назначать пробиотики и другие «профилактические» препараты всем людям, принимающим антибиотики.
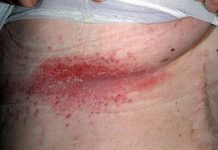
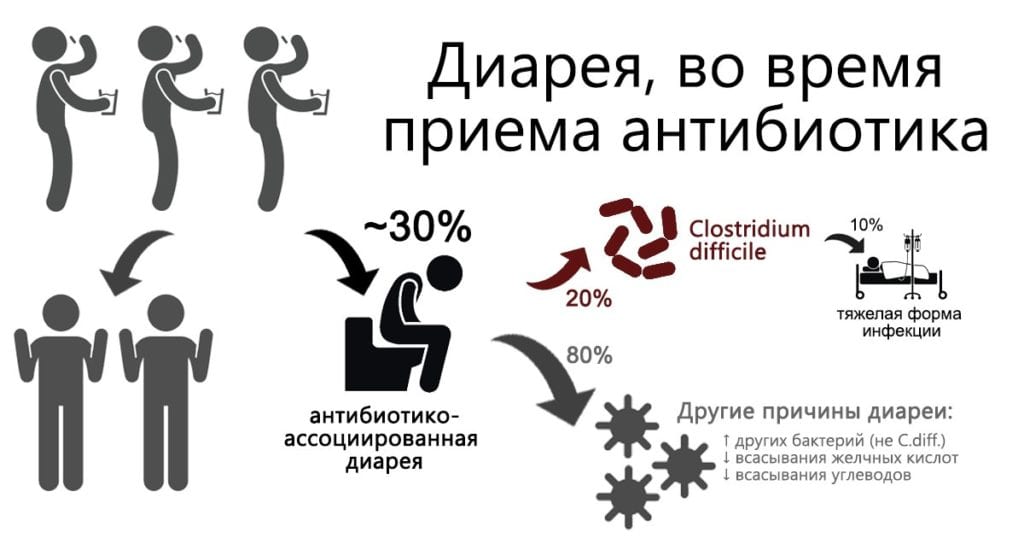
Диарея при приеме антибиотиков – частое и нередко неизбежное явление. Диарея возникает у 5-39% взрослых и у 11-40% детей, принимающих антибиотики. Диарея может появиться даже спустя 2 месяца после начала их приема. Большинство случаев антибиотико-ассоциированной диареи, к нашему счастью, протекают легко (без подъема температура, потери белка и т.п.) и заканчиваются самостоятельно без всякого лечения.
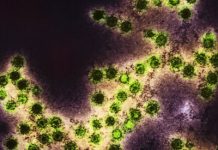
Главную опасность представляет инфекция бактерией Clostridium difficile. Она обитает в кишечнике, как минимум, каждого пятого человека, не вызывая симптомов. С этой бактерией конкурируют нормальные бактерии пищеварительного тракта, не давая ей размножаться и выделять токсины. После приема антибиотиков состав кишечной микрофлоры меняется, «конкуренты» погибают, и усиливается рост C.difficile . Она выделяет токсины А и В, вызывающие выброс жидкости в просвет кишки (токсин действует как осмотическое слабительное типа пикосульфата) и воспаление (токсин напрямую повреждает клетки слизистой оболочки кишечника). В последнее время появился особо опасный штамм бактерии (NAP1/027), выделяющий бинарный токсин, ~в 10 раз сильнее действующий на кишечную стенку. И это проблема.
В чем опасность C.difficile?
У 20% людей проявления инфекции C.difficile проходят сами после отмены антибиотика, у остальных диарея и другие симптомы сохраняются. У части людей с инфекцией развивается псевдомембранозный колит — воспаление толстой кишки: частота колеблется от 10% до 40%. Псевдомембранозный колит — серьезное состояние: смертность при нем составляет не менее 10%. Псевдомембранозный колит повышает вероятность тяжелых осложнений заболевания: токсической дилатации (паралитического расширения толстой кишки, которое может привести к перфорации и перитониту), серьезной анемии и гипопротеинемии (потере белка) и сепсиса. При развитии осложнений и неэффективности лечения приходится выполнять колэктомию — удалять толстую кишку. Смертность в такой ситуации взлетает до 80%.
Главная «проблема» с C.difficile — то, что в нашем распоряжении очень мало способов справиться с инфекцией. Однозначно эффективны только метронидазол, ванкомицин (его в этой ситуации дают строго внутрь, а не внутривенно!) и фидаксомицин. Последний в России не зарегистрирован и продается в Европе по ~1000 EUR на курс терапии. Очень эффективна трансплантация фекальной микробиоты (по-простому, введение фекалий здорового человека пациенту), но в России царит законодательный «вакуум» (методика не лицензирована) и эту процедуру проводили на свой страх и риск лишь отдельные клиники (включая автора этого текста).
Понос во время приема антибиотиков — всегда от этой страшной Clostridium difficile?
К счастью, нет. Большинство случаев диареи (75-80%), вызванной антибиотиками, не связаны с C.difficile. Эти случаи может быть связано с реакцией собственно на препарат (например, на клавулановую кислоту в составе Амоксиклава, раздражающую слизистую оболочку). Кроме того, неспецифические изменения микрофлоры кишечника могут приводить к уменьшению всасывания некоторых углеводов, а также желчных кислот — «естественных» слабительных нашего организма. Это временные явления.
Но перестраховаться же можно?Если C.difficile размножается от недостатка конкурентов, надо их в кишку «подсадить» — принимать пробиотики?
Мы не уверены, что это необходимо всем. В декабре 2017 г был опубликован очередной Кокрановский систематический обзор. В нем были обобщены результаты 39 рандомизированных исследований у 8672 пациентов, получавших пробиотики, чтобы защититься от инфекции C.difficile во время терапии антибиотиком. Авторы обнаружили, что терапия пробиотиками снижает вероятность инфекции только у людей из «группы риска» — тех, у кого вероятность C.difficile-инфекции превышает 5% (скажем, у пожилых пациентов с ослабленным иммунитетом). При исходно низком риске (у молодых пациентов без хронических заболеваний) дополнительный прием пробиотика не влиял на вероятность диареи.
Based on this systematic review and meta-analysis of 31 randomizedcontrolled trials including 8672 patients, moderate certainty evidence suggests that probiotics are effective for preventing CDAD (NNTB = 42 patients, 95% CI 32 to 58). Our post hoc subgroup analyses to explore heterogeneity indicated that probiotics are effective among trials with a CDAD baseline risk >5% (NNTB = 12; moderate certainty evidence), but not among trials with a baseline risk ≤5% (low to moderate certainty evidence). Although adverse effects were reported among 32 included trials, there were more adverse events among patients in the control groups. The short-term use of probiotics appears to be safe and effective when used along with antibiotics in patients who are not immunocompromised or severely debilitated. Despite the need for further research, hospitalized patients, particularly those at high risk of CDAD, should be informed of the potential benefits and harms of probiotics.
Далеко не все исследования профилактического приема пробиотиков спланированы и проведены качественно и однотипно, так что обобщать их выводы трудно. Кроме того, большая часть этих работ выполнены у пациентов, более подверженных клостридиальной инфекции, чем «среднестатистический» потребитель антибиотиков. В двух наиболее крупных рандомизированных исследованиях пробиотиков при рутинном назначении антибиотика их эффективность не была подтверждена. В первом из них (2900 пациентов) эффект от приема комбинированного пробиотика (Lactobacillus acidophilus и Bifidobacterium bifidum) был таким же, как и прием плацебо (пустышки): диарея появилась у сопоставимого числа участников. Во втором исследовании пациенты получали или плацебо, или дрожжевой грибок Saccharomyces boulardii. Результаты тоже разочаровали: прием пробиотика на риск диареи, вызванной антибиотиком, не влиял.
Я запутался(лась). Надо все-таки пить пробиотики одновременно с антибиотиками?
Всем подряд – нет! Потратить деньги на пробиотик имеет смысл только тем, у кого вероятна инфекция Clostridium difficile. Эта инфекция относится к нозокомиальным (внутрибольничным), то есть шанс заразиться ей выше в лечебном учреждении, особенно в стационаре. Помимо пребывания на больничной койке, к другим факторам риска C.difficile-инфекции относятся:
- Серьезные хронические заболевания (по-видимому, два и более; например, неконтролируемый диабет и хроническая почечная недостаточность)
- Возраст старше 65 лет
- Воспалительные заболевания кишечника (язвенный колит и болезнь Крона)
- Длительный прием ингибиторов протонной помпы (например, омепразола)
- Лечение препаратами, подавляющими иммунитет (азатиоприном, метотрексатом, циклоспорином, такролимусом, глюкокортикостероидами)
- Химиотерапия
Именно в подобных случаях дополнительный прием пробиотика оправдан и, по-видимому, эффективен.
Хорошо, посоветую своей бабушке с диабетом попить йогурт, когда ей назначат антибиотики. В нем же много полезных бактерий, так?
Не все «йогурты» одинаково полезны. Строго говоря, обычные йогурты для профилактики клостридиальной диареи бесполезны. Потенциально эффективны только бактерии Lactobacillus acidophilus, L. casei и L. rhamnosus, а также дрожжи Saccharomyces boulardii (Энтерол), причем последний пробиотик, по-видимому, наиболее эффективен.
Эффективный пробиотик («полезный» микроорганизм) должен как-то оказаться в кишечнике, преодолев естественный барьер – кислую среду в желудке. В желудке значительная часть пробиотика неизбежно погибнет. По этой причине пробиотики необходимо давать в большой дозе – более 10 миллиардов КОЕ в день.
КОЕ – колониеобразующая единица – соответствует одной жизнеспособной бактерии.
Из популярных российских бактериальных пробиотиков (препаратов лактобактерий) такая концентрация в инструкции заявлена только у препаратов Бифиформ-малыш, Линекс-форте и Лактобактерин.
А противогрибковые средства надо принимать? Вдруг от антибиотика у меня в кишке размножатся грибы?
Противогрибковые препараты (например, флуконазол) принимать не надо. Антибиотик, меняя состав кишечной микрофлоры, может вызвать временное увеличение грибков, например, Candida. Но диарея от этого не возникает. Австрийцы оценили рост этого грибка у людей принимавших антибиотики, сопоставив его с теми, кто антибиотики не принимал. Избыточный рост Кандиды действительно чаще отмечался у принимавших антибиотики. Вот только степень ее размножения, а также продукция грибков токсина — аспартил-протеиназы, были одинаковыми у людей с диареей, вызванной антибиотиком, и у людей, у которых прием антибиотика не вызвал жидкого стула. В общем, кандида-то есть, но диарею она не вызывает. А «инвазивные» кандидозы, к счастью для нас, не развиваются у людей без тяжелого иммунодефицита.
Ну и, естественно, ни одно руководство даже не упоминает необходимость принимать противогрибковые препараты одновременно с антибиотиками.
В общем:
Если антибиотик назначен не госпитализированному пожилому пациенту, человеку с воспалительным заболеванием кишечника и другими серьезными сопутствующими заболеваниями, не получающему иммуносупрессоры или химиопрепараты, профилактический прием пробиотиков не нужен. Жидкий стул может появиться и пройдет самостоятельно без остаточных явлений. Если жидкий стул возникает чаще чем три раза в день и не проходит в течение 3 дней, есть повод проконсультироваться с врачом, главным образом, чтобы выполнить анализ кала на токсины C.difficile.
Ну, а главная профилактика антибиотико-ассоциированной диареи — рационально использовать антибиотики, скажем, не пить их при «простуде» (чаще всего, вирусном заболевании).
А про «анализ кала на дисбактериоз» — следующий пост
Не болейте!